据日本共同社报道,由专家组成的审查委员会已批准两项基于诱导性多能干细胞(iPS细胞)的医疗产品。若获得卫生大臣最终批准,这些产品将成为全球首例获批的iPS细胞治疗产品。目前审查遵循日本的有条件批准制度,即便获批上市,仍需对产品进行长达七年的安全性和有效性追踪研究。
两项产品分别为用于心脏病患者的心肌细胞贴片和用于帕金森病患者的多巴胺能神经元细胞。心肌贴片由大阪大学衍生的初创企业Cuorips Inc.开发,多巴胺能神经元则由住友制药株式会社研制。iPS细胞通过提取患者自身或其他人细胞制备,理论上可减少排斥反应,但长期安全性仍是行业挑战。
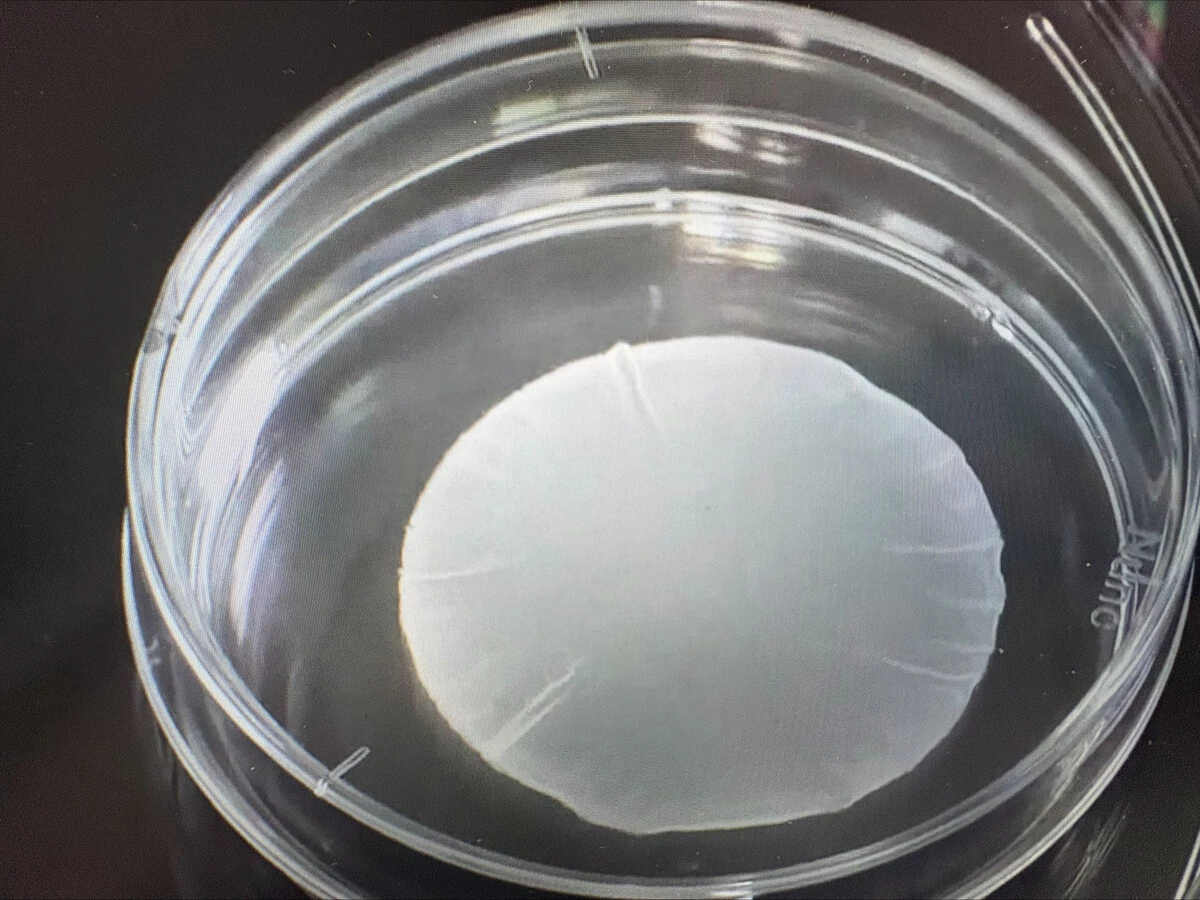
2020年,大阪大学团队首次将iPS细胞心肌贴片移植至缺血性心肌病引发心力衰竭的患者体内。截至2023年,该团队已对8名患者进行测试,确认产品安全有效。贴片直径4-5厘米,厚度约0.1毫米。
针对帕金森病的多巴胺能神经元治疗则由京都大学医院等机构自2018年起在50-60岁患者中开展。研究团队向患者脑部移植约500万至1000万个神经细胞。经两年观察,6名患者中有4人运动功能显著改善,且未出现严重副作用,年轻症状较轻的患者疗效更佳。
[版权信息:日本共同社]